进行了研究以确定用于多潘立酮 API 的最佳激光衍射粒度分散方法。
本研究采用了Bettersizer 2600——一种具有干湿分散系统的自动激光衍射粒度分析仪——使研究人员能够系统地研究多潘立酮 API 的粒度分布。
此处介绍的研究检查了分散强度对粒度分析的影响,采用一系列不同的气压进行干分散,采用一系列不同的超声波分散时间和搅拌速度进行湿分散。
对湿式和干式分散方法的测量结果进行了比较,发现湿式分散方法最合适,因为它具有准确结果和数据相关性的能力。
多潘立酮的作用
多潘立酮主要作用于血脑屏障外的化学感受器触发区域。它是第二代胃动力剂的一个例子——一种合成的苯并咪唑衍生物。
多潘立酮是一种多巴胺受体阻滞剂,通过阻断外周多巴胺受体来帮助抑制呕吐,增强胃动力,同时增加下食管括约肌压力。
多潘立酮尚未获得美国食品和药物管理局 (FDA) 的批准,但可在其他地方广泛使用。
它最常用于治疗由化疗引发的食管反流、胀气和呕吐。
多潘立酮颗粒的溶解度是其被人体吸收能力的关键因素,这意味着了解颗粒大小对整体产品质量的影响至关重要。
批次间粒度分布的差异导致体内溶出和吸收不一致,直接影响药物的疗效和安全性。
USP 提供了关于使用激光衍射的 API 粒度的明确规定。例如,提供了有关仪器结构和原理、干湿分散的具体方法以及在测量过程中应考虑的一系列因素的信息。
然而,对于特定药物的湿法或干法分散方法的选择没有指导,也没有关于评估该决定的信息。
本文详细介绍了在测量多潘立酮原料药粒度分布时选择合适的分散方法的系统研究。这符合 USP 和 ISO 13320 的要求。
实验
仪器
本实验使用Bettersize Instruments Ltd.的Bettersizer 2600激光粒度分析仪、Mettler Toledo的MS303S电子秤和上海盛研超声波仪器有限公司的SC超声波清洗机。
样品和试剂
本研究使用了两组多潘立酮 API 样品:
非微粉样品(批号0068116-17)
微粉化样品
吐温 80 用作分析试剂。还使用了纯净水。
粒度分布测量及方法评价:干法分散法
干式分散使用压缩空气来输送粉末颗粒,颗粒通过相互碰撞、与管道碰撞以及气流剪切的组合进行分散。
API 粉末通常由易于因碰撞和剪切应力而破裂的有机小分子颗粒组成。尽管如此,重要的是确保大团块的分散而不破坏原始颗粒。
因此,USP 促使调查色散强度对测试结果的影响 (USP 429)。

在本研究期间进行的干分散实验中,根据分散压力对粒度结果的影响来评估分散压力的影响。分散压力范围从 0.05 MPa 到 0.4 MPa,每 0.05 MPa 测试一组数据。
呈现的结果包括:
横坐标:分散压力
纵坐标:粒度
蓝色曲线:D10
橙色曲线:D50
灰色曲线:D90
理想的压力滴定曲线将显示粒径随着分散压力的增加而逐渐减小。曲线将逐渐达到稳定期。
但是,如果压力增加超过该点,则曲线将进一步向下移动,对应于大团聚体逐渐分散为单个颗粒。压力的任何进一步增加都可能导致药物颗粒破裂。
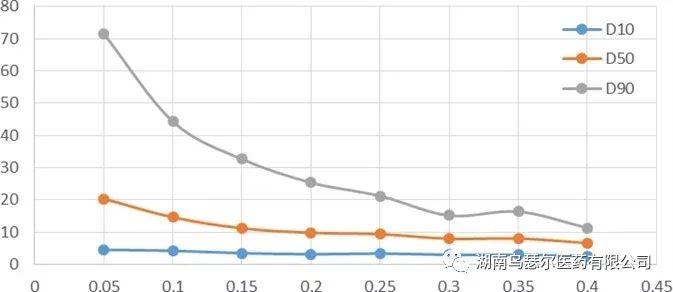
药物粒度测定的一个关键挑战在于聚集体分散和单颗粒破碎之间缺乏严格的界限。为了探索这一点,还需要进一步的实验。
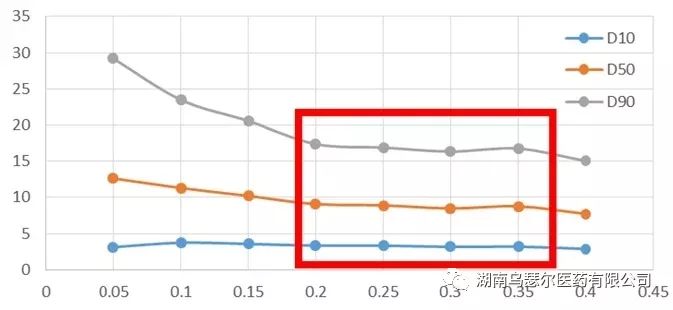
在0.2-0.35 MPa之间观察到微粉样品(图2)明显的稳定平台,但进一步增加非微粉样品的压力导致没有稳定平台,导致样品粒径不断减小。这通常是颗粒破损的迹象。

捕获非微粉化样品(图 3)的图像以进行进一步研究,确认样品由半透明的不规则晶体颗粒组成。对这些图像的评估表明,随着干燥分散压力的增加,样品很容易破裂。
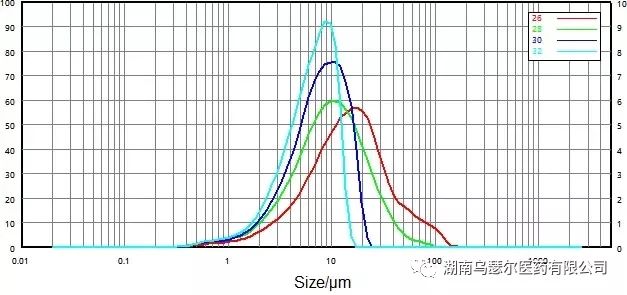
在不同压力下评估非微粉化样品的粒度分布(图 4),以确定最佳干分散压力。结果表明,随着分散压力的增加,最大粒径从 150-100 µm 减少到 30-20 µm。
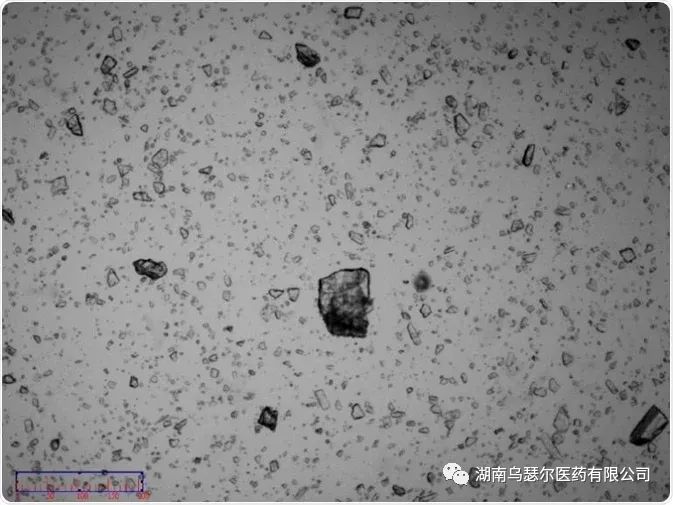

样品图像证实存在一些尺寸约为 100 µm 的粗颗粒。这些粗颗粒是单个颗粒而不是团聚颗粒(图 5 和图 6)。
这些粒径约为 100 µm 的颗粒的存在否定了最大粒径为 30-20 µm 的断言。然而,可以得出结论,当分散压力达到 0.3 MPa 及以上时,颗粒会破裂。
压力滴定曲线(图 2)和样品的脆性导致决定使用 0.2 MPa 的压力来测试多潘立酮 API 的粒度分布。
干法分散法的精度
在 0.2 MPa 的分散压力下测量多潘立酮 API。图 7 和图 8 显示了非微粉化和微粉化样品的粒度分布曲线和重复性数据。
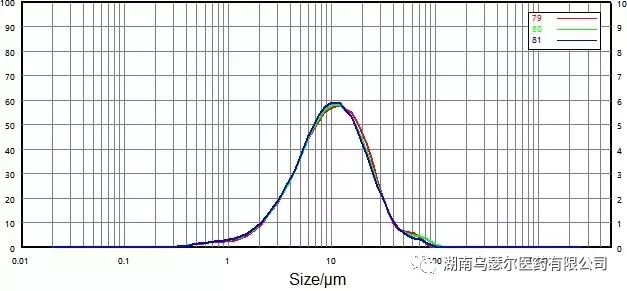
|
79 | 0068116-17 非微粉化-0.2 | 3.332 | 10.31 | 26.44 |
80 | 0068116-17 非微粉化-0.2 | 3.222 | 10.13 | 26.79 |
81 | 0068116-17 非微粉化-0.2 | 3.157 | 9.905 | 25.91 |
标准差 |
| 2.73% | 2.01% | 1.68% |
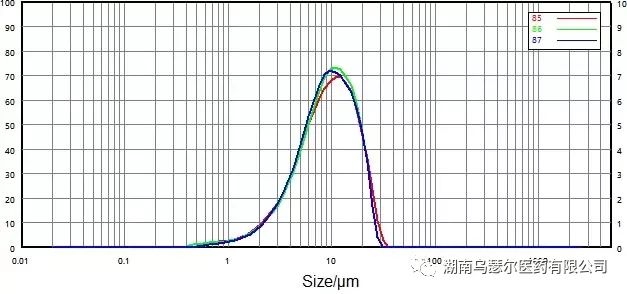
|
85 | 0068116-17 微粉化-0.2 | 3.274 | 9.341 | 19.27 |
86 | 0068116-17 微粉化-0.2 | 3.398 | 9.377 | 18.63 |
87 | 0068116-17 微粉化-0.2 | 3.505 | 9.174 | 18.60 |
标准差 |
| 3.41% | 1.17% | 2.01% |
图 8.微粉化颗粒的粒径分布和重复性(干分散)
两个样品的重复性轻松超过 USP 中概述的要求:D50 的重复性小于 2.1%,而 D10 和 D90 的重复性小于 3.5%。
这些值证实干法分散法是测量多潘立酮 API粒度分布的可靠方法。
粒度分布测量和方法评价:湿法分散法
多潘立酮 API 不溶于水,这意味着在通过搅拌和超声分散分散在水中之前,它必须用表面活性剂润湿。它的脆性意味着分散强度低。
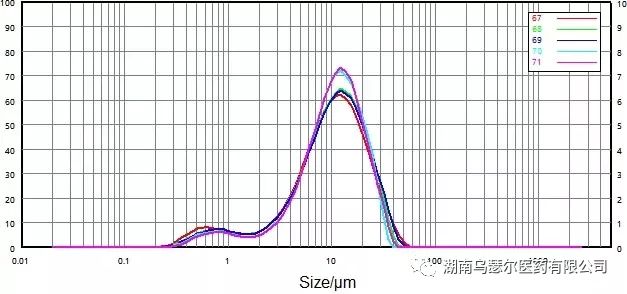
|
67 | 0068116-17 微粉化-B | 2.066 | 10.14 | 24.21 |
68 | 0068116-17 微粉化-B | 2.481 | 10.49 | 23.71 |
69 | 0068116-17 微粉化-B | 2.514 | 10.622 | 4.57 |
70 | 0068116-17 微粉化-B | 3.127 | 10.63 | 22.06 |
71 | 0068116-17 微粉化-B | 3.297 | 10.74 | 22.54 |
标准差 |
| 18.75% | 2.21% | 4.61% |
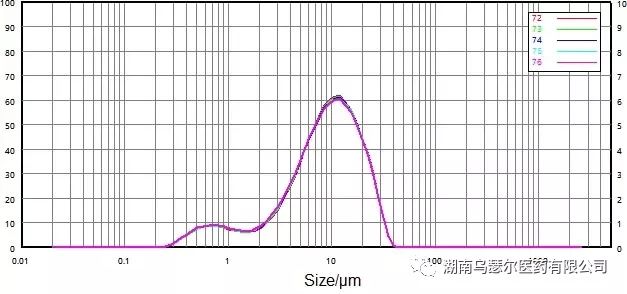
|
72 | 0068116-17 微粉化-C | 1.719 | 9.200 | 21.35 |
73 | 0068116-17 微粉化-C | 1.716 | 9.154 | 21.31 |
74 | 0068116-17 微粉化-C | 1.660 | 9.120 | 21.32 |
75 | 0068116-17 微粉化-C | 1.666 | 9.089 | 21.32 |
76 | 0068116-17 微粉化-C | 1.616 | 9.031 | 21.25 |
标准差 |
| 2.57% | 0.70% | 0.17% |
图 10.仅搅拌分散后的测试样品粒度分布。
分别应用搅拌和超声分散方法(图 9 和图 10)来确定分散强度对样品颗粒的影响。
仅对样品应用搅拌方法时,结果不稳定,湿分散的特性意味着药物颗粒仍然可以粘附。
然而,在低强度超声分散后稳定性显着提高。超声波分散对粒度分布的影响最小——其主要影响是大颗粒拖尾。
低强度超声分散下的重复性也大大提高,因此决定在随后的湿法分散中采用低强度超声方法。
湿法分散法的精度
使用上述相同的实验条件,对通过低强度超声分散样品进行分散时粒度分布数据的精度进行了调查。
|
96 | 0068116-17 非微粉化-C | 2.632 | 11.68 | 32.51 |
97 | 0068116-17 非微粉化-C | 2.640 | 11.69 | 32.29 |
98 | 0068116-17 非微粉化-C | 2.627 | 11.66 | 32.30 |
99 | 0068116-17 非微粉化-C | 2.615 | 11.60 | 31.96 |
100 | 0068116-17 非微粉化-C | 2.552 | 11.44 | 30.91 |
标准差 |
| 1.35% | 0.89% | 1.99% |
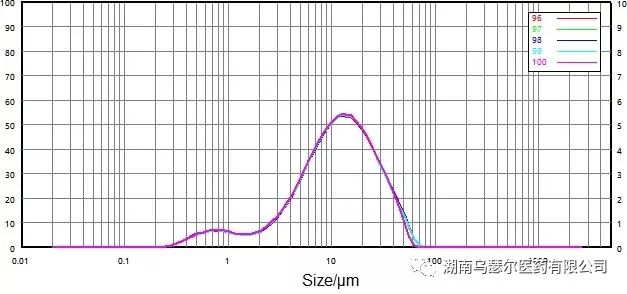
图 11.非微粉化样品(湿分散)的粒度分布和可重复性。
|
78 | 0068116-17 微粉化-C | 1.611 | 9.008 | 21.29 |
79 | 0068116-17 微粉化-C | 1.595 | 8.971 | 21.28 |
80 | 0068116-17 微粉化-C | 1.579 | 8.945 | 21.22 |
81 | 0068116-17 微粉化-C | 1.570 | 8.944 | 21.28 |
82 | 0068116-17 微粉化-C | 1.561 | 8.916 | 21.23 |
标准差 |
| 1.26% | 0.39% | 0.15% |
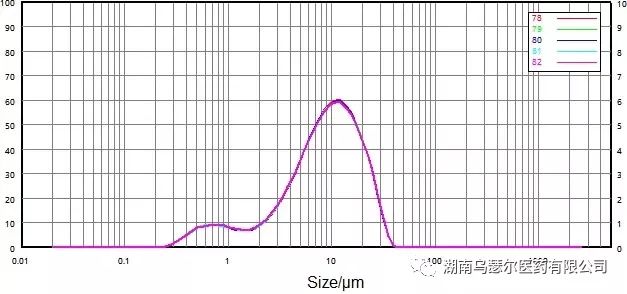
图 12.微粉化样品的粒度分布和重复性(湿分散)。
图 11 和图 12 都显示了非微粉化和微粉化样品的湿分散的粒度分布和可重复性数据。
与干分散体相比,重复性大大提高:D50 和 D90 的相对偏差小于 0.7%,而 D10 的相对偏差小于 2.6%。
这些发现证实,对于多潘立酮 API 粒度分布的测量,湿分散比干分散更可靠。
干湿分散方法的比较与评价
就测试精度而言,湿法分散是比干法分散更好的选择。这是因为颗粒在干分散过程中仅通过测试区域一次,而湿分散则使它们反复通过。这导致湿分散期间更高的采样频率。
|
82 | 0068116-17 微粉化-C | 1.561 | 8.916 | 21.23 |
100 | 0068116-17 非微粉化-C | 2.552 | 11.44 | 30.91 |
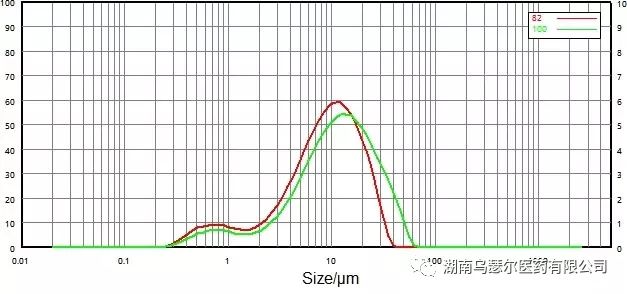
图 13.比较微粉化前后的粒度分布结果(湿法分散)。

|
81 | 0068116-17 非微粉化-0.2 | 3.157 | 9.905 | 25.91 |
86 | 0068116-17 微粉化-0.2 | 3.398 | 9.377 | 18.63 |
图 14.比较微粉化前后的粒度分布结果(干分散)。
图 13 和图 14 显示了通过干法和湿法分散方法获得的非微粉化和微粉化样品的粒度分布数据。
就数据的相对合理性而言,湿法分散法在微粉化后粒径分布峰向更小的颗粒移动。D10、D50、D90均有不同程度的下降。
然而,对于干法分散方法,大颗粒在微粉化之前和之后都发生了显着变化,而细颗粒几乎没有变化。
结论
这些实验证实,湿法和干法分散法均可为测定多潘立酮 API 的粒径分布提供高精度结果。
由于多潘立酮 API很脆弱,因此需要更多关于样品分散选择的数据,特别是对于干分散方法。
在这些实验中,发现湿法分散提供的数据与通过干法分散提供的数据相比具有更高的可重复性、相关性和合理性。
因此,可以得出结论,湿法分散法是分析多潘立酮 API 粒度分布的良好选择。